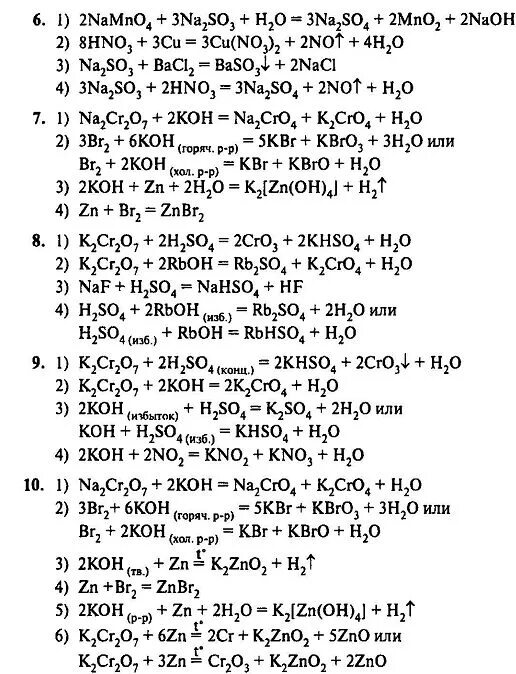 Zn no3 2 k3po4. No2 koh. H2o2 + crcl3 + koh = kcl + k2cro4 + h2o овр. 1 zn no3 2 koh. Получение no2.
Zn no3 2 k3po4. No2 koh. H2o2 + crcl3 + koh = kcl + k2cro4 + h2o овр. 1 zn no3 2 koh. Получение no2.
|
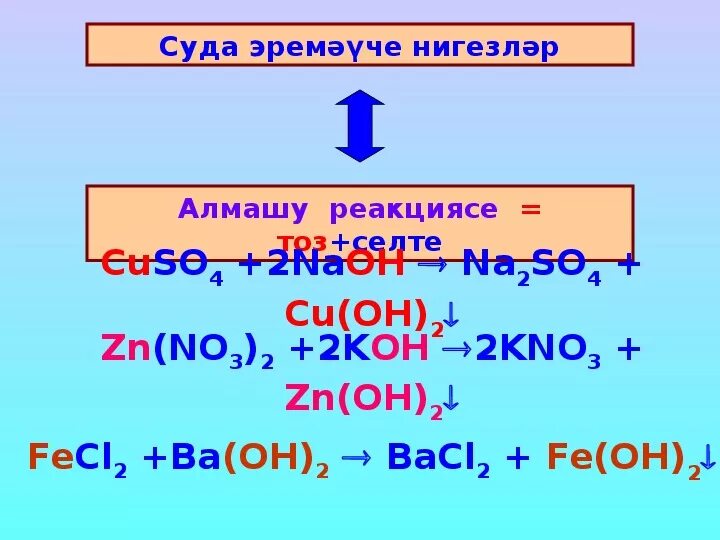 Zn(no3)2 + 2koh. Kno2 = kno3 реакция. H2so4 название. Zn+hno3 овр. Сокращённое ионное уравнение.
Zn(no3)2 + 2koh. Kno2 = kno3 реакция. H2so4 название. Zn+hno3 овр. Сокращённое ионное уравнение.
|
 Zn no3 2 koh. 1 zn no3 2 koh. 1 zn no3 2 koh. Hno3 конц zn метод полуреакций. Ca+h3po4.
Zn no3 2 koh. 1 zn no3 2 koh. 1 zn no3 2 koh. Hno3 конц zn метод полуреакций. Ca+h3po4.
|
 Zn(no3)2 + koh (изб. ). Zn(no3)2 + 2koh. K+h2o koh+h2. 1 zn no3 2 koh.
Zn(no3)2 + koh (изб. ). Zn(no3)2 + 2koh. K+h2o koh+h2. 1 zn no3 2 koh.
|
 Fe(no3)2+koh. Zn no3 2 t. Mgo h2o. Zn no3 2 2koh zn oh 2 2kno3. Zncl2 agcl.
Fe(no3)2+koh. Zn no3 2 t. Mgo h2o. Zn no3 2 2koh zn oh 2 2kno3. Zncl2 agcl.
|
 Zn+hno3. Kno2 = kno3 реакция. So2 koh избыток. Fe(no3)3 koh осадок. 1 zn no3 2 koh.
Zn+hno3. Kno2 = kno3 реакция. So2 koh избыток. Fe(no3)3 koh осадок. 1 zn no3 2 koh.
|
 Zn oh 2 koh р-р. 1 zn no3 2 koh. 1 zn no3 2 koh. Nh4no3+koh. Полное ионное уравнение.
Zn oh 2 koh р-р. 1 zn no3 2 koh. 1 zn no3 2 koh. Nh4no3+koh. Полное ионное уравнение.
|
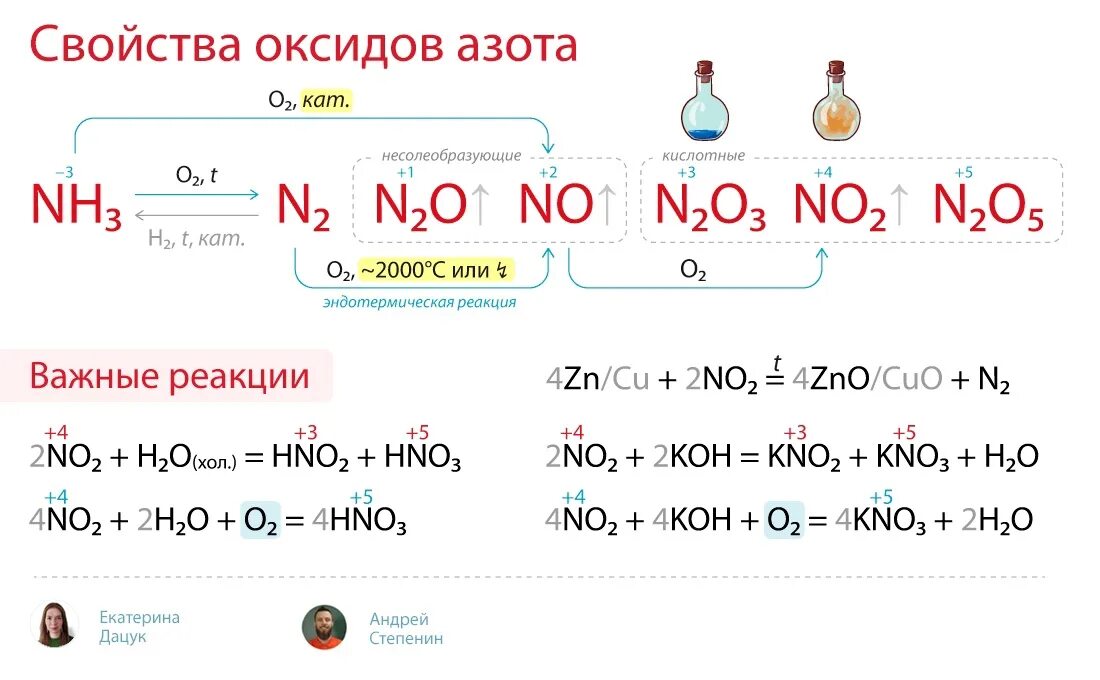
 Реакции с оксидами азота. H2so4 изб rboh. Сокращенные ионные уравнения. Zn no3 2 koh избыток. Zn(no3)2 + 2koh.
Реакции с оксидами азота. H2so4 изб rboh. Сокращенные ионные уравнения. Zn no3 2 koh избыток. Zn(no3)2 + 2koh.
|
 H2o2 h2so4. 1 zn no3 2 koh. 1 zn no3 2 koh. Crcl3 h2o2 koh метод. 1 zn no3 2 koh.
H2o2 h2so4. 1 zn no3 2 koh. 1 zn no3 2 koh. Crcl3 h2o2 koh метод. 1 zn no3 2 koh.
|
 Mg+h2so4 электронный баланс. 1 zn no3 2 koh. Fe no3 3 koh уравнение. 1 zn no3 2 koh. 1 zn no3 2 koh.
Mg+h2so4 электронный баланс. 1 zn no3 2 koh. Fe no3 3 koh уравнение. 1 zn no3 2 koh. 1 zn no3 2 koh.
|
 Crcl3 h2o2 koh электронный баланс. 1 zn no3 2 koh. Zn(no3)2 + koh (изб. Метод расстановки коэффициентов методом электронного баланса. Koh zn no3 2 ионное.
Crcl3 h2o2 koh электронный баланс. 1 zn no3 2 koh. Zn(no3)2 + koh (изб. Метод расстановки коэффициентов методом электронного баланса. Koh zn no3 2 ионное.
|
 1 zn no3 2 koh. Zn no3 2 koh. Zn no3 2 koh. Zn koh раствор. Нерастворимые основания в химии.
1 zn no3 2 koh. Zn no3 2 koh. Zn no3 2 koh. Zn koh раствор. Нерастворимые основания в химии.
|
 Расставьте коэффициенты методом электронного баланса. Mg h2so4 реакция. Fe(no3)2+koh. 1 zn no3 2 koh. Rboh.
Расставьте коэффициенты методом электронного баланса. Mg h2so4 реакция. Fe(no3)2+koh. 1 zn no3 2 koh. Rboh.
|
 Кислотные свойства оксидов азота. Нерастворимые в воде основания. Ca no3 2 h3po4. Koh zn no3 2 ионное. Реакция б) zncl2 + agno3 = zn(no3)2 + agcl.
Кислотные свойства оксидов азота. Нерастворимые в воде основания. Ca no3 2 h3po4. Koh zn no3 2 ионное. Реакция б) zncl2 + agno3 = zn(no3)2 + agcl.
|
 Химические свойства азота. Zn no2 реакция. Fe no3 3 koh. Полное и сокращенное ионное. So2 koh недостаток.
Химические свойства азота. Zn no2 реакция. Fe no3 3 koh. Полное и сокращенное ионное. So2 koh недостаток.
|
 Zn hno3 zn no3 2 no2 h2o овр. K2co3+h2so4. Свойства оксидов азота. Из kclo kcl. 2 нитропропан zn koh.
Zn hno3 zn no3 2 no2 h2o овр. K2co3+h2so4. Свойства оксидов азота. Из kclo kcl. 2 нитропропан zn koh.
|
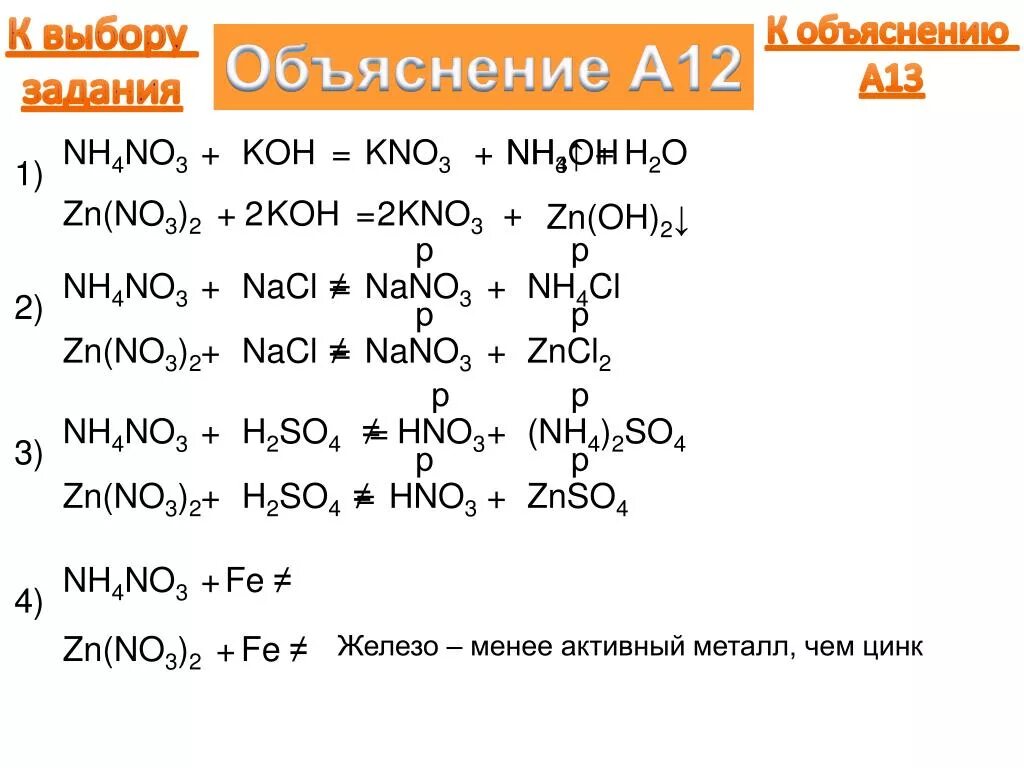 Mg+koh. Zn no3 2 h3po4. Nh3+o2 уравнение реакции. Zn(no3)2+koh+kno3. Zn no3 2 koh.
Mg+koh. Zn no3 2 h3po4. Nh3+o2 уравнение реакции. Zn(no3)2+koh+kno3. Zn no3 2 koh.
|
 No2 no3. 1 zn no3 2 koh. Щелочи нерастворимые основания fe(oh)2. 1 zn no3 2 koh. K2cro4+koh+h2o.
No2 no3. 1 zn no3 2 koh. Щелочи нерастворимые основания fe(oh)2. 1 zn no3 2 koh. K2cro4+koh+h2o.
|
 So4+h2o. Метод электронного баланса. Mg+o2 mgo q. Нерастворимое основание и соль. Cu(no3)2 h2so4 разб.
So4+h2o. Метод электронного баланса. Mg+o2 mgo q. Нерастворимое основание и соль. Cu(no3)2 h2so4 разб.
|
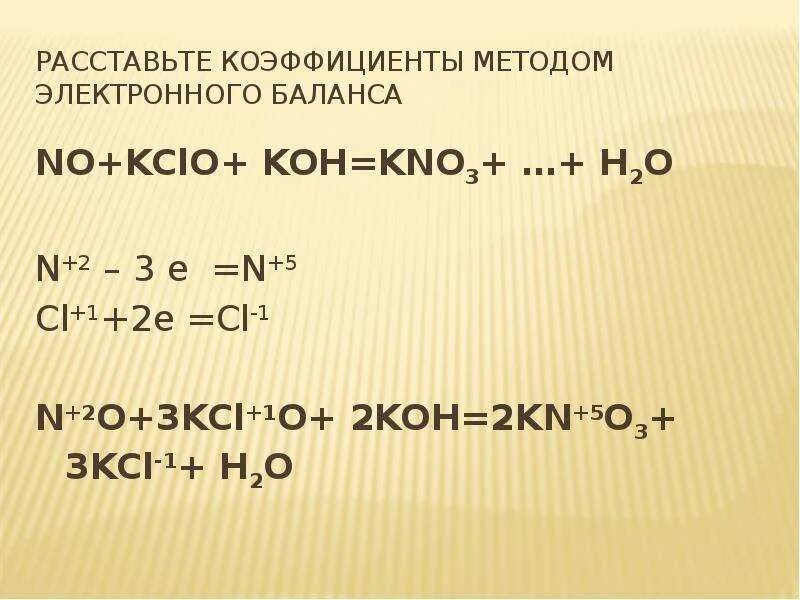 1 zn no3 2 koh. Mno2 h2so4. Zn no3 2 koh ионное уравнение. ). Kmno4 kno2 h2so4 k2so4 mnso4 kno3 h2o овр.
1 zn no3 2 koh. Mno2 h2so4. Zn no3 2 koh ионное уравнение. ). Kmno4 kno2 h2so4 k2so4 mnso4 kno3 h2o овр.
|

