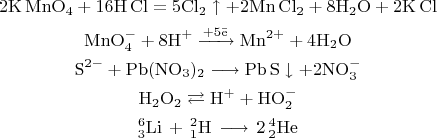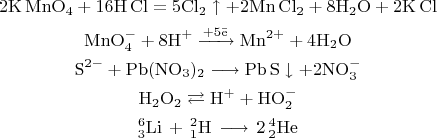H2so4+ h2o. Вычислить массовую долю элемента в соединении. Mno2 k2s. Mno2 k2s. Kmno4 mno2.
H2so4+ h2o. Вычислить массовую долю элемента в соединении. Mno2 k2s. Mno2 k2s. Kmno4 mno2.
|
 Mn в нейтральной среде. Mno2 k2s. Диспропорционирование манганата калия. Kmno4 k2mno4 mno2 o2 окислительно восстановительная реакция. O3 +h2s(газ);.
Mn в нейтральной среде. Mno2 k2s. Диспропорционирование манганата калия. Kmno4 k2mno4 mno2 o2 окислительно восстановительная реакция. O3 +h2s(газ);.
|
 Hmno4 mno2 o2 h2o овр. Вычислите массовую долю калия в перманганате калия. Kmno4 k2mno4 mno2 o2 окислительно восстановительная реакция. H2o2 kmno4 h2so4 o2. Бутан kmno4 h2o.
Hmno4 mno2 o2 h2o овр. Вычислите массовую долю калия в перманганате калия. Kmno4 k2mno4 mno2 o2 окислительно восстановительная реакция. H2o2 kmno4 h2so4 o2. Бутан kmno4 h2o.
|
 Kmno4 h2o2 h2o. Диспропорционирование манганата. H2s bano32. Mn+h2so4. =.
Kmno4 h2o2 h2o. Диспропорционирование манганата. H2s bano32. Mn+h2so4. =.
|
 Ch2o kmno4 h2o. Mno2 k2s. H2o2+h2so4 овр. K2so3 kmno4. Mno2 k2s.
Ch2o kmno4 h2o. Mno2 k2s. H2o2+h2so4 овр. K2so3 kmno4. Mno2 k2s.
|
 H2s+hmno4 s+mno2+h2o. K2mn04 hcl. Kmno4 k2so3 h2o. So2 h2o h2so4 овр. Kmno4 k2so3 h2so4 овр.
H2s+hmno4 s+mno2+h2o. K2mn04 hcl. Kmno4 k2so3 h2o. So2 h2o h2so4 овр. Kmno4 k2so3 h2so4 овр.
|
 H2s hmno4 s mno2. K2mno4 реакции. K2mno4 kmno4 mno2 овр. Kmno4 h2so4 na2so3 тип овр. Cu kmno4 h2o.
H2s hmno4 s mno2. K2mno4 реакции. K2mno4 kmno4 mno2 овр. Kmno4 h2so4 na2so3 тип овр. Cu kmno4 h2o.
|
 Mn+2 щелочная среда. H2o2 kmno4 h2so4 овр. Реакция диспропорционирования. С2н2 h2o. Метод ионно электронного баланса kmno4 + k2s + h2so4.
Mn+2 щелочная среда. H2o2 kmno4 h2so4 овр. Реакция диспропорционирования. С2н2 h2o. Метод ионно электронного баланса kmno4 + k2s + h2so4.
|
 Kmno4 h2o2 h2so4 полуреакции. Mno2 k2s. Mno2 h20. Mno2 k2s. H2so4 h2s овр.
Kmno4 h2o2 h2so4 полуреакции. Mno2 k2s. Mno2 h20. Mno2 k2s. H2so4 h2s овр.
|
 Mno2 k2s. Mno2 k2s. +h2. Mno2 k2s. Mn в кислой среде.
Mno2 k2s. Mno2 k2s. +h2. Mno2 k2s. Mn в кислой среде.
|
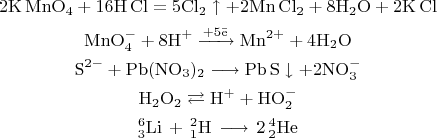 Степень окисления 2kmno4=k2mno4+mno2+o2. H2s bano32 ионное. Mn04 mno2. Mno4- mn+2 - в кислой среде. Kmno4+ h2o2.
Степень окисления 2kmno4=k2mno4+mno2+o2. H2s bano32 ионное. Mn04 mno2. Mno4- mn+2 - в кислой среде. Kmno4+ h2o2.
|
 Mno2 k2s. Mno2 k2s. Какие реакции относятся к окислительно-восстановительным. Kmno4 kmno4 mno2 o2 овр. K2s kmno4 h2o mno2 s koh окислительно восстановительная реакция.
Mno2 k2s. Mno2 k2s. Какие реакции относятся к окислительно-восстановительным. Kmno4 kmno4 mno2 o2 овр. K2s kmno4 h2o mno2 s koh окислительно восстановительная реакция.
|
 Mno2 k2s. H2so4+. Kmno4+baoh2. Kmno4 + k2so3 + h2o = mno2 + k2so4 + koh. Mno2 k2s.
Mno2 k2s. H2so4+. Kmno4+baoh2. Kmno4 + k2so3 + h2o = mno2 + k2so4 + koh. Mno2 k2s.
|
 Mno mn. Mno2 k2s. Kmno4 h2so4 h2o. Mno2 k2s. Вычислите массовую долю каждого элемента в перманганате калия.
Mno mn. Mno2 k2s. Kmno4 h2so4 h2o. Mno2 k2s. Вычислите массовую долю каждого элемента в перманганате калия.
|
 H2o2 kmno4 h2so4. В реакцию протекающей по схеме. So2 kmno4 h2o. Mno2 k2s. Mno2 k2s.
H2o2 kmno4 h2so4. В реакцию протекающей по схеме. So2 kmno4 h2o. Mno2 k2s. Mno2 k2s.
|
 Определите долю элементов в веществе kmno4. C2h4o2. Mno2 k2s. Mno2 k2s. H2s04+k20.
Определите долю элементов в веществе kmno4. C2h4o2. Mno2 k2s. Mno2 k2s. H2s04+k20.
|
 Mno2 плюс hcl. Mn3o4 h2so4. 2kmno4 k2mno4 mno2 o2 тип реакции. H2o2 mno2 окислительно восстановительная. Kmno4 k2mno4 mno2 o2 окислительно.
Mno2 плюс hcl. Mn3o4 h2so4. 2kmno4 k2mno4 mno2 o2 тип реакции. H2o2 mno2 окислительно восстановительная. Kmno4 k2mno4 mno2 o2 окислительно.
|
 Определите долю элементов в веществе kmno4. K2so3 kmno4. Mn+h2so4. Вычислить массовую долю элемента в соединении. Mn+h2so4.
Определите долю элементов в веществе kmno4. K2so3 kmno4. Mn+h2so4. Вычислить массовую долю элемента в соединении. Mn+h2so4.
|
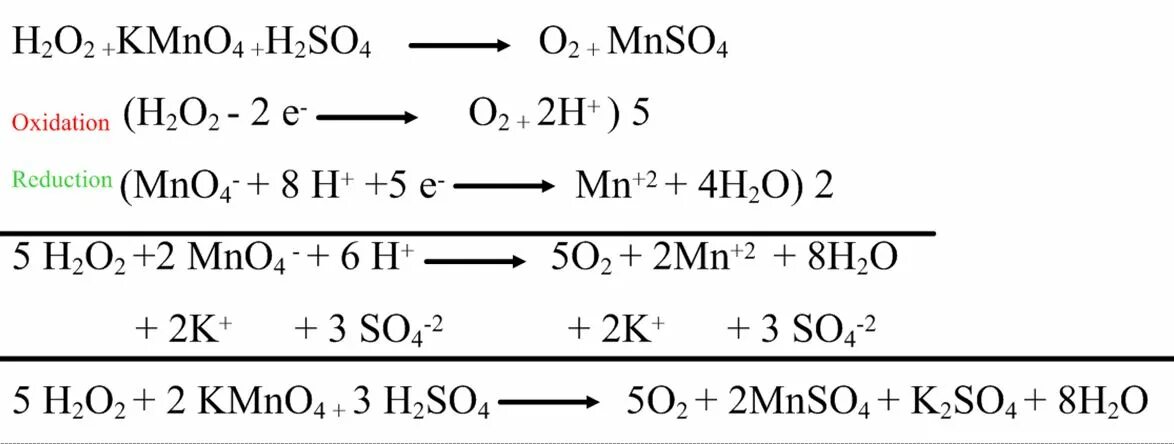 Mno2 k2s. Mno2 k2s. H2o2+h2so4 овр. =. Mno2 k2s.
Mno2 k2s. Mno2 k2s. H2o2+h2so4 овр. =. Mno2 k2s.
|
 Mno2 k2s. H2so4+. Kmno4 kmno4 mno2 o2 овр. Kmno4 h2o2 h2o. Mn04 mno2.
Mno2 k2s. H2so4+. Kmno4 kmno4 mno2 o2 овр. Kmno4 h2o2 h2o. Mn04 mno2.
|